



Aan deze uitwerking kunnen geen rechten worden ontleend
Voor de pijnbestrijding bij een ernstig zieke patient schrijft de behandelend arts capsules met de volgende samenstelling voor:
oxycodon hydrochloride 5 mg
Omdat dit preparaat in de toekomst vaker gebruikt zal worden wordt de bruikbaarheid van het bereidingsvoorschrift onder meer gecontroleerd door tien capsules met HPLC te analyseren. De uitkomsten hiervan staan vermeld in de onderstaande tabel.
acetylsalicylzuur 250 mg
microkristallijne cellulose ad capsules nr 2
|
capsule |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
acetylsalicylzuur (mg) |
210 |
189 |
240 |
289 |
235 |
212 |
224 |
251 |
255 |
256 |
|
oxycodon HCl (mg) |
4.11 |
3.44 |
4.57 |
5.34 |
4.78 |
4.26 |
4.47 |
5.10 |
5.19 |
4.95 |
Vraag 1
a. Wijken de gemiddelde gehalten voor acetylsalicylzuur en oxycodonhydrochloride in dit preparaat significant (95% betrouwbaarheid) af van het gedeclareerd gehalte ?
Omdat hier sprake is van een verdeeld geneesmiddel is de Q-test niet van toepassing.
Berekening via de t-toets geeft aan dat de t-waarde beneden de kritische waarde 2.26 (tweezijdig 95% betrouwbaarheid, 9 vrijheidsgraden) ligt:
|
t-waarde oxycodonhydrochloride |
2.07 |
|
t-waarde acetylsalicylzuur |
1.53 |
Berekening van de betrouwbaarheidsintervallen van het gemiddeld gehalte geeft aan dat de gedeclareerde waarden daarbinnen liggen.
|
|
gemiddeld gehalte |
standaardafwijking |
betrouwbaarheidsinterval (95%, tweezijdig) |
|
acetylsalicylzuur |
236 |
28.7 |
216-257 |
|
oxycodonhydrochloride |
4,62 |
0,579 |
4.21-5.03 |
b. Is voor dit preparaat onderzoek naar de gelijkmatigheid van gehalte vereist volgens de Europese Farmacopee?
Ja, in de monografieën voor verdeelde geneesmiddelvormen wordt een onderzoek naar de Uniformity of Content geëist indien het gehalte aan werkzaam bestanddeel 2 mg of minder en/of minder dan 2% bedraagt.
c. Zou dit preparaat aan de eisen voor gelijkmatigheid van gehalte voldoen ?
|
capsule |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
oxycodon HCl (mg) |
4.11 |
3.44 |
4.57 |
5.34 |
4.78 |
4.26 |
4.47 |
5.10 |
5.19 |
4.95 |
|
afwijking in % |
-11 |
-26 |
-1 |
16 |
3 |
-8 |
-3 |
10 |
12 |
7 |
Van de tien capsules wijkt er 1 meer dan 25% af. Dit betekent, dat al na het onderzoek van 10 capsules vastgesteld kan worden dat de capsules niet aan de eisen van gelijkmatigheid van gehalte voldoen
Vraag 2.
Kleine hoeveelheden zijn over het algemeen moeilijker homogeen over een massa te verdelen dan grote hoeveelheden.
a. Geven de analyseresultaten aanleiding om te veronderstellen dat de grotere hoeveelheid acetylsalicylzuur meer homogeen verdeeld is dan het oxycodonhydrochloride ?
De relatieve standaarddeviatie in het acetylsalicylzuurgehalte bedraagt 12,2%. Die in het oxycodongehalte bedraagt 12,5%. Deze spreidingen zijn ongeveer even groot. Bovendien zou, indien de homogene verdeling van het oxycodonhydrochloride problematisch zou zijn, de spreiding in de verhouding van de beide gehalten per capsule groter moeten zijn dan die in de bestanddelen afzonderlijk.
Het is bij de onderzochte capsules echter zo dat de capsules die weinig oxycodonhydrochloride bevatten ook overeenkomstig weinig acetylsalicylzuur bevatten .
|
capsule |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
verhouding acetylsalicylzuur -codeine |
51.09 |
54.94 |
52.52 |
54.12 |
49.16 |
49.77 |
50.11 |
49.22 |
49.13 |
51.72 |
Gemiddeld bedraagt de verhouding van de gehalten 51.18. De relatieve standaarddeviatie hierin bedraagt 4,1%.
b. Zou de spreiding in de gevonden gehalten bij deze capsules te wijten zijn aan een verschil in de mate van vulling of aan problemen bij de menging van de werkzame bestanddelen en de hulpstoffen ? Onderbouw uw conclusie statistisch.
Indien op de relatieve standaarddeviatie van het acetylsalicylzuurgehalte en die van de verhouding van de beide gehalten een F-test wordt uitgevoerd, wordt een waarde van 8.68 gevonden. Deze waarde is groter dan de waarde 4.03 uit de tabel (tweezijdig, 95% betrouwbaarheidsinderval).
Voor oxycodonhydrochloride wordt op analoge wijze 9.22 gevonden, hetgeen eveneens boven de kritische waarde ligt.
Dit betekent dat de spreiding in het aceylsalicylzuurgehalte significant groter is, dan die in de verhouding van de gehalten van acetylsalicylzuur en codeine per capsule.
Indien er een mengprobleem was opgetreden, zou de spreiding in de verhouding van de beide bestanddelen groter moeten zijn, dan de spreiding in de gehalten afzonderlijk. Kennelijk is hier niet het mengen, maar het vullen van de capsules het probleem. Nader onderzoek naar de gewichtsspreiding zou dat dan moeten bevestigen.
Vraag 3.
Is het mogelijk bij dit preparaat het gehalte aan acetylsalicylzuur spectrofotometrisch te bepalen door het oplossen van de capsule-inhoud in alcohol en vervolgens de extinctie te meten bij 278 nm ? Geef aan in welke mate het oxycodonhydrochloride hierbij stoort.
De storing van de oxycodonhydrochloride bedraagt ongeveer 44 / 68 x 5 / 250 = 1,3%.
Vraag 4.
Voor het onderzoek naar de afgiftesnelheid worden de capsules in een acetaatbuffer van pH 4.5 gebracht en wordt de concentratie van het vrijgekomen acetylsalicylzuur en het oxycodon na 30 min. gemeten. Overeenkomstig de eis van de U.S.P. moet na 30 min. tenminste 80% van het oxycodonhydrochloride en ten minste 75% van het acetylsalicylzuur uit de capsules vrijgekomen zijn.
Geef aan op welke wijze u de concentratie van het vrijgekomen acetylsalicylzuur, inclusief het door voorafgaande of tussentijdse ontleding ontstane salicylzuur, spectrofotometrisch met één enkele meting kwantitatief als acetylsalicylzuur kunt bepalen.
Door te meten bij een golflengte waarbij de molaire extincties van acetylsalicylzuur en salicylzuur gelijk zijn (isosbestisch punt) kan de totale hoeveelheid van het acetylsalicylzuur die oorspronkelijk aanwezig was, berekend worden uit één enkele meting. Het is echter ook mogelijk het gehalte te meten door de oplossingen alkalisch te maken en na enige wachttijd (de hydrolyse van acetylsalicylzuur verloopt in alkalisch milieu zeer snel) het ontstane salicylaat bij 300 nm te meten. Deze golflengte heeft tevens het voordeel dat de storing door het oxycodonhydrochloride geëlimineerd wordt.
Vraag 5.
De verantwoordelijke analist maakt voor het onderzoek naar de afgiftesnelheid van acetylsalicylzuur een ijklijn voor de spectrofotometer. Hij is van mening dat het geavanceerde apparaat dat hij gebruikt ook metingen buiten het bereik van 0,2 tot 0,8 extinctie-eenheden mogelijk maakt. De meetresultaten worden in de bijlage gegeven.
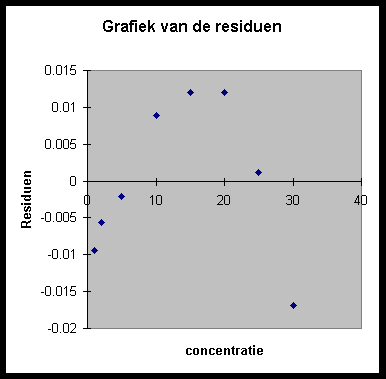
Wijzen de meetresultaten uit dat het apparaat binnen het gebruikte bereik lineair is ?/I>
Uit de verschillen tussen de gemeten en de berekende waarden blijkt dat deze verschillen (residuen) niet random verdeeld zijn. Er is dus sprake van een afwijking van de lineariteit.
|
concentratie in mg/ 100 ml |
gemeten |
berekend |
verschil |
|
1 |
0.067 |
0.076 |
-0.009 |
|
2 |
0.137 |
0.143 |
-0.006 |
|
5 |
0.339 |
0.341 |
-0.002 |
|
10 |
0.681 |
0.672 |
0.009 |
|
15 |
1.015 |
1.003 |
0.012 |
|
20 |
1.346 |
1.334 |
0.012 |
|
25 |
1.666 |
1.665 |
0.001 |
|
30 |
1.979 |
1.996 |
-0.017 |
De navolgende grafiek illustreert dit nog duidelijker.
Vraag 6.
Voor de HPLC-bepaling van oxycodon vindt u in de literatuur de onderstaande twee loopmiddelen voor gebruik op een SelectB-kolom.
a. Voorspel het chromatografisch gedrag van de stoffen oxycodon, acetylsalicylzuur en het ontledingsproduct salicylzuur met loopmiddel 1.
Bij dit loopmiddel zal oxycodon als ionpaar retentie ondervinden. Acetylsalicylzuur en salicylzuur zullen retentie ondervinden als ongedissociëerde zuren. Salicylzuur zal hierbij door de intramoleculaire waterstofbrug meer retentie vertonen dan acetylsalicylzuur. Op grond van de structuur is het moeilijk om te voorspellen wat het verschil in retentie van oxycodon en acetylsalicylzuur is. (Experimenteel onderzoek zou in dit geval uitwijzen, dat de retentie van acetylsalicylzuur aanzienlijk groter is dan die van oxycodon).
b. Voorspel het chromatografisch gedrag van de stoffen oxycodon, acetylsalicylzuur en het ontledingsproduct salicylzuur met loopmiddel 2.
Bij dit loopmiddel zullen acetylsalicylzuur en salicylzuur nagenoeg volledig gedeprotoneerd (en daardoor geladen) zijn en dientengevolge nauwelijks retentie ondervinden. Zij worden daardoor sneller geëlueerd dan het oxycodon, dat, omdat het voor een aanzienlijk gedeelte ongeladen is, juist extra retentie ondervindt.
c. Geef aan naar welk van deze beide loopmiddelen uw voorkeur voor de bepaling van oxycodon zou uitgaan en beargumenteer uw keuze.
Bij gebruik van het tweede loopmiddel worden acetylsalicylzuur en salicylzuur op de dode tijd geëlueerd. Hierdoor worden zij gescheiden van de oxycodon zonder dat zij de analyseduur verlengen of mogelijkerwijze met de oxycodonpiek samenvallen.
Vraag 7.
a. Geef aan hoe u het acetylsalicylzuur uit de capsules in voldoend zuivere, droge vorm zou isoleren om er een IR-spectrum van op te nemen.
Door droge extractie met ether wordt het acetylsalicylzuur in zuivere vorm verkregen. Microkristallijne cellulose lost hierin niet op. Oxycodonhydrochloride lost niet in de ether op, maar zou in de gedeclareerde concentratie overigens toch niet storen. Het gebruik van ether heeft vanwege het lage kookpunt heeft de voorkeur boven een oplosmiddel als ethanol.
b. Geef aan hoe u het oxycodon (als base) in voldoend zuivere, droge vorm uit de capsules zou isoleren om er een IR-spectrum van op te nemen.
Door de capsule-inhoud met verdund zwavelzuur te extraheren wordt het oxycodon in oplossing gebracht. Het microkristallijne cellulose en het grootste deel van het acetylsalicylzuur gaan hierbij niet in oplossing. Na filtreren of centrifugeren wordt de verkregen oplossing alkalisch gemaakt en geëxtraheerd met chloroform of dichloormethaan. Eventuele sporen (acetyl)salicylzuur worden gedeprotoneerd en blijven daardoor in de waterlaag achter. Na wassen met water en drogen over watervrij natriumsulfaat wordt de organische laag ingedampt. Het verkregen residu wordt gebruikt voor het opnemen van het IR-spectrum.
Vraag 8.
Vanwege de bij de patiënt optredende misselijkheid stelt de behandelend arts voor om over te gaan op zetpillen met dezelfde gehalten aan werkzame stoffen.
Geef aan hoe in de werkzame bestanddelen uit de matrix (adeps solidus) zou isoleren voorafgaande aan een HPLC-bepaling.
Bij extractie in een systeem bestaande uit petroleumether en 70% alcohol gaan de werkzame bestanddelen over in de 70% alcohollaag en de vette bestanddelen in de petroleumether. De alcohollaag kan vervolgens met HPLC worden onderzocht. Voor een kwantitatieve bepaling is meervoudige extractie aan te bevelen. Bovendien dient dan een controle op de volledigheid van de extractie uitgevoerd te worden.
Vraag 9.
a. Geef aan u hoe de identiteit van de vetzuren in de tri- en diglyceriden in adeps solidus zou kunnen bepalen.
Bij hydrolyse in een methanolische kaliloog worden methylesters gevormd. Deze kunnen na extractie met hexaan of heptaan gaschromatografisch worden aangetoond.
Het is ook mogelijk de vetzuren na een hydrolyse in waterig milieu met HPLC op een reversed phase kolom aan te tonen (detectie met een refractometer of met UV bij 210 nm).
b. Geef aan op welke wijze u de aanwezigheid van diglyceriden in adeps solidus zou kunnen aantonen.
Bij chromatografie op silicagel worden de triglyceriden en diglyceriden als groepen van elkaar gescheiden. Hierbij treedt ook scheiding op tussen de 1,2-diglyceriden en de 1,3-diglyceriden.
25 januari 2002
Staf Farmaceutische Analyse 5e-jaar