



Beantwoord de onderstaande vragen en licht de antwoorden toe, ook wanneer dat niet expliciet gevraagd wordt.
Twee apothekers, verbonden aan verschillende ziekenhuizen, laten ampullen, die bereid zijn volgens het bijgevoegde voorschrift, analyseren door een onafhankelijk laboratorium. Zij leveren ieder een zestal ampullen uit een door hen zelf bereide charge. Het controlelaboratorium past hierbij als analysemethode UV-spectrometrie en HPLC toe. De gevonden resultaten staan vermeld in de onderstaande tabel
|
|
Uitkomst UV-bepaling mg/ml |
Uitkomst HPLC-bepaling mg/ml |
|
Ziekenhuis 1 |
|
|
|
ampul 1 |
0.248 |
0.239 |
|
ampul 2 |
0.244 |
0.240 |
|
ampul 3 |
0.250 |
0.248 |
|
ampul 4 |
0.258 |
0.246 |
|
ampul 5 |
0.247 |
0.246 |
|
ampul 6 |
0.246 |
0.253 |
|
|
|
|
|
Ziekenhuis 2 |
|
|
|
ampul 1 |
0.257 |
0.244 |
|
ampul 2 |
0.249 |
0.236 |
|
ampul 3 |
0.245 |
0.233 |
|
ampul 4 |
0.257 |
0.244 |
|
ampul 5 |
0.255 |
0.242 |
|
ampul 6 |
0.258 |
0.245 |
Vraag 1
a. Bepaal het gemiddelde en de standaardafwijking in de monsters per ziekenhuis per bepalingsmethode.
|
|
Uitkomst UV-bepaling mg/ml |
Uitkomst HPLC-bepaling mg/ml |
|
Ziekenhuis 1 |
|
|
|
gemiddelde |
0.2488 |
0.2453 |
|
standaarddeviatie |
0.0049 |
0.0052 |
|
|
|
|
|
Ziekenhuis 2 |
|
|
|
gemiddelde |
0.2535 |
0.2407 |
|
standaarddeviatie |
0.0053 |
0.0050 |
b. Bereken of de gehalten van de ampullen van ziekenhuis tot ziekenhuis significant verschillen (alfa=0,05) en motiveer de keuze van de statistische toets.
De vergelijking tussen de ziekenhuizen geschiedt met een ongepaarde t-toets omdat hiermee kan worden vastgesteld of de verschillen in de gemiddelden significant zijn gezien de spreiding in de uitkomsten per ziekenhuis.
|
|
UV-bepaling |
HPLC-bepaling |
|
gepoolde standaarddeviatie |
0.0051 |
0.0051 |
|
t-berekend |
1.58 |
1.59 |
Voor beide bepalingsmethoden geldt dat de berekende t-waarde kleiner is dan 2,23.
c. Bereken of de uitkomsten van de twee bepalingsmethoden significant verschillen (alfa=0,05) en motiveer de keuze van de statistische toets.
De vergelijking geschiedt hier bij voorkeur met een gepaarde t-toets. Hierbij wordt het effect van een eventuele spreiding in het gehalte van de ampullen binnen één charge geëlimineerd. Men zou hier tegen in kunnen brengen, dat binnen een charge van ampullen die bereid zijn uit dezelfde homogene oplossing geen verschillen in gehalte zouden mogen optreden (men houdt dan echter geen rekening met een eventuele ontleding tijdens de sterilisatie) en dat een ongepaarde t-toets ook acceptabel zou moeten zijn.
Berekening met de gepaarde t-toets
|
ziekenhuis1 |
ziekenhuis 2 |
|
|
ampul 1 |
0.009 |
0.013 |
|
ampul 2 |
0.004 |
0.013 |
|
ampul 3 |
0.002 |
0.012 |
|
ampul 4 |
0.012 |
0.013 |
|
ampul 5 |
0.001 |
0.013 |
|
ampul 6 |
-0.007 |
0.013 |
|
gemiddelde verschil |
0.0035 |
0.0128 |
|
standaarddeviatie |
0.0067 |
0.0004 |
|
standaarddeviatie in gemiddelde |
0.0027 |
0.0002 |
|
t-berekend |
1.29 |
77 |
Uit de gevonden waarden blijkt dat bij de ampullen van het tweede ziekenhuis de HPLC bepaling uitkomsten geeft die significant verschillen van die van de UV-bepaling (t-waarde van de tabel 2.57 tweezijdig 95% betrouwbaarheidsinterval, 5 vrijheidsgraden).
Berekening met de ongepaarde t-toets
|
|
gepoolde standaarddeviatie |
t-berekend |
|
Ziekenhuis 1 |
0.0051 |
1.20 |
|
Ziekenhuis 2 |
0.0051 |
4.34 |
Uit de vonden waarden blijkt dat bij de ampullen van het tweede ziekenhuis de HPLC bepaling uitkomsten geeft die significant verschillen van die van de UV-bepaling (t-waarde van de tabel bedraagt 2,23 voor een tweezijdig 95% betrouwbaarheidsinterval met 10 vrijheidsgraden).
d. Beredeneer welke bepalingmethode de meest betrouwbare informatie over het atropinegehalte geeft.
Atropine is een ester die potentieel kan hydrolyseren. Het is denkbaar dat de charge van het tweede ziekenhuis ouder is en daardoor voor een deel gehydrolyseerd, of dat bij de sterilisatie in verschillende mate hydrolyse opgetreden is. Bij de UV-bepaling worden atropine en het hydrolyseproduct tropazuur in gelijke mate bepaald. Bij de HPLC-bepaling wordt alleen het atropine bepaald. De HPLC-bepaling geeft daardoor betrouwbaarder informatie over het atropinegehalte dan de UV-bepaling
Mesalamineklysma
U krijgt opdracht een mesalamineklysma te onderzoeken. Het bereidingsvoorschrift staat vermeld in de bijlage.
Vraag 2
a. Geef aan met welke functionele groepen de genoemde pKa-waarden corresponderen en geef aan hoe de lading van het mesalaminemolecule over het pH-gebied 0-14 varieert.
De pKa-waarden worden volgens het onderstaande schema aan de functionele groepen toegerekend.
|
groep |
pKa-waarde |
|
carboxylgroep |
2,3 |
|
aminogroep |
5,69 |
|
fenolgroep |
13,9 |
De lading van het mesalaminemolecule wordt in de onderstaande tabel beschreven.
|
pH-gebied |
lading |
|
< 2.3 |
+ |
|
2.3-5.69 |
0 (zwitterion) |
|
5.69-13.9 |
- |
|
>13.9 |
2- |
b. Geef aan hoe u mesalamine uit dit preparaat moet isoleren om er een IR-spectrum van op te nemen.
Uit het voorschrift voor de bereiding en uit de gegeven oplosbaarheid blijkt dat hier sprake is van een suspensie.
Door centrifugeren van de suspensie en uitwassen van het neerslag kan het mesalamine op eenvoudige wijze geïsoleerd worden. Na drogen kan dan het IR-spectrum opgenomen worden.
c. Bereken de specifieke extinctie van mesalamine bij de absorptiemaxima uit het bijgevoegde spectrum.
De berekende specifieke extincties staan weergegeven in de onderstaande tabel.
|
230 nm |
464 |
|
300 nm |
214 |
d. Leg uit of het mogelijk is om mesalamine in dit preparaat zonder voorafgaande isolatie via UV te bepalen ?
Van de begeleidende stoffen vertoont alleen methylparahydroxybenzoaat UV-absorptie. Deze absorptie is echter te verwaarlozen bij 300 nm, waar mesalamine het tweede absorptiemaximum heeft. Bovendien is mesalamine bijna 30x hoger gedoseerd dan methylparahydroxybenzoaat. De voor analyse van mesalamine benodigde concentratie is zo laag, dat de oplosbaarheid er van voldoende groot is. Het kan dus bepaald worden door de suspensie eenvoudig te verdunnen en de extinctie te meten bij 300 nm.
e. Geef aan met welke testen u aannemelijk kunt maken dat in het preparaat carbomeer verwerkt is.
De viscositeit van de oplossing is een indicatie voor de aanwezigheid van verdikkingsmiddel. De pH-afhankelijkheid van de viscositeit is een indicatie voor de aanwezigheid van carbomeer. Daarnaast kan de aanwezigheid van carbomeer aannemelijk worden gemaakt door het neerslag dat met calciumionen ontstaat.
f. Geef aan op welke wijze u uit dit preparaat methylparahydroxybenzoaat kunt isoleren ten behoeve van DLC.
Voor deze isolatie ligt een extractie met ether vanuit zuur milieu voor de hand.
Vraag 3
a. Leg uit welk van de beide loopmiddelen u zou gebruiken om mesalamine te analyseren met HPLC op een Select B-kolom:
- een mengsel van methanol en water óf
- een mengsel van methanol en water waaraan 0.01 M. perchloorzuur is toegevoegd.
In een water-methanol mengsel zonder toevoegingen is de pH niet gedefiniëerd. Onder die omstandigheden gedraagt mesalamine zich onvoorspelbaar.
Door een toevoeging van perchloorzuur wordt de carboxylgroep van het mesalamine geprotoneerd. Het ontstane kation (kan als ionpaar met perchloraat gechromatografeerd worden.
b. Beredeneer welk(e) ontledingsproduct(en) u bij mesalamine moet verwachten.
De aanwezigheid van een fenolgroep en een aminogroep in para-positie ten opzichte van elkaar in het molecule van mesalamine maakt deze stof zeer oxidabel. Bovendien is aanwezigheid van het antioxidans natriummetabisulfiet is een indicatie voor het risico van oxidatieve ontleding.
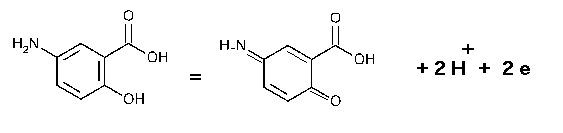
c. Geef de reactievergelijking voor deze ontleding en geef aan of de ontleding bij hoge pH sneller of langzamer verloopt.
Hierbij kan de 4-aminofenolstructuur overgaan in een chinoïde structuur. Bij deze oxidatie komen twee protonen en twee electronen vrij. Het vrijkomen van protonen brengt met zich mee, dat deze oxidatie bij hogere pH sneller verloopt.
d. Beredeneer waar de piek(en) van deze ontledingsproduct(en) op het chromatogram verwacht moet(en) worden.
Uit de structuur van het oxidatieproduct blijkt dat dit minder polair is dan mesalamine. Het zal dus in het gebruikte HPLC-systeem meer retentie vertonen.
Natriumchloride oogzalf
Het bereidingsvoorschrift van de natriumchlorideoogzalf staat vermeld in de bijlage.
Vraag 4
a. Geef aan op welke wijze natriumchloride uit deze oogzalf geïsoleerd kan worden.
Voor de isolatie uit een vette matrix wordt over het algemeen petroleumether als apolaire fase gebruikt.
Gezien het polaire karakter van natriumchloride kan hier als polaire fase water gebruikt worden.
Gebruik van een mengsel van water met methanol of ethanol is hier strikt genomen niet nodig.
Gezien het polaire karakter van het natriumchloride zou in dit geval een systeem bestaande uit ether of chloroform en water ook voldaan hebben.
b. Leg uit hoe in deze zalf het natriumchloride bepaald kan worden via het natrium-ion.
Het natriumchloride kan bepaald worden door het waterige extract aan AES te onderwerpen
c. Leg uit hoe in deze zalf het natriumchloride titrimetrisch bepaald kan worden via het chloride-ion. Beschrijf het titrans, het milieu en de eindpuntsindicatie.
Voor de titratie van chloride ligt het titrans zilvernitraat voor de hand.
Deze titratie kan op de volgende manieren uitgevoerd worden:
1. Titreren in zuur milieu met een potentiometrische eindpuntsindicatie met behulp van een zilverelectrode als indicator-electrode en een double junction referentie-electrode.
2. Titreren in neutraal milieu met kaliumdichromaat als indicator (titratie volgens Mohr)
3. Toevoegen van een overmaat zilvernitraat gevolgd door een terugtitratie in zuur milieu met thiocyanaat met ferriammoniumsulfaat als indicator (omslag van kleurloos naar rood). Hierbij dient het gevormde zilverchloride door schudden met dibutylftalaat 'omhuld' te worden, waardoor het niet door het titrans omgezet kan worden in het iets slechter oplosbare zilverthiocyanaat (titratie volgens Volhard.)
d. Geef aan op welke wijze de hulpstoffen in dit preparaat aangetoond kunnen worden en welk analyseresultaat u hierbij krijgt.
Voor de karakerisering van de hulpstoffen kan het best DLC op silicagel (vettenplaat) gebruikt worden. Hierbij vertoont wolvet een karakteristiek patroon van vlekken. Cetostearylalcohol geeft één vlek omdat er geen verschil in gedrag is tussen hexadecanol en octadecanol. De detectie geschiedt bij voorkeur met anilinonaftaleensulfonzuur of met jodiumdamp.
Vaseline en paraffine geven vlekken die zeer dicht bij het front liggen. Deze beide stoffen kunnen dan ook op deze manier niet van elkaar onderscheiden worden.
Met gaschromatografie kunnen hexadecanol en octadecanol geïdentificeerd worden. De vloeibare paraffine geeft hierbij een brede piek die veroorzaakt wordt door de afzonderlijke pieken van de samenstellende alkanen.
25 juni 2001
Staf Farmaceutische Analyse 5e-jaar