



|
monster genomen midden boven |
monster genomen midden onder |
monster genomen zijkant boven |
monster genomen zijkant onder |
|
101,8 |
101,9 |
97,3 |
99,0 |
|
102,7 |
104,4 |
97,1 |
99,9 |
|
102,1 |
101,3 |
99,5 |
100,8 |
|
99,4 |
101,2 |
97,8 |
99,7 |
|
99,5 |
100,4 |
99,9 |
98,1 |
|
99,3 |
102,3 |
100,1 |
79,9 |
a. Is er bij dit onderzoek sprake van uitbijters ?
Indien de waarden van de vierde reeks op volgorde van toenemende waarde gerangschikt worden wordt de reeks 79,9 - 98,1 - 99,0 - 99,7 - 99,9 - 100,8 verkregen. De Q-test levert (98,1 - 79,9)/(100,8 - 79,9) = 0,871. Deze waarde is groter dan de kritische waarde 0,628 (95% betrouwbaarheid) en zelfs groter dan 0,740 (99% betrouwbaarheid). De waarde 79,9 wordt daarom verworpen.b. Bereken per monsterplaats het gemiddelde gehalte en de standaardafwijking
|
|
monster genomen midden boven |
monster genomen midden onder |
monster genomen zijkant boven |
monster genomen zijkant onder |
|
gemiddelde |
100,8 |
101,9 |
98,6 |
99,5 |
|
standaardafwijking |
1,56 |
1,38 |
1,37 |
1,01 |
|
interval 95% betrouwbaarheid voor het gemiddelde |
99,16 - 102,44 |
100,47 - 103,36 |
97,18 - 100,05 |
98,24 - 100,76 |
Toepassing van de F-toets op de twee standaarddeviaties die het meest verschillen (1,56 en 1,01) levert de waarde 2,39 op. Deze waarde ligt ver beneden de kritische waarde voor de F-toets 9,36 (serie met 5 en met 4 vrijheidsgraden respectievelijk). De berekende waarde 2,39 is zelfs kleiner dan 7,15 (voor twee series met ieder 5 vrijheidsgraden). Het berekenen van de gepoolde standaarddeviaties levert daardoor geen problemen op.2. Een apotheker wil voor kaliumsuppletie een kaliumdrank bereiden die minder onaangenaam smaakt. Hij vervangt daarom een deel van het kaliumchloride door kaliumgluconaat. Hij levert het mengsel van kaliumchloride en kaliumgluconaat in verdeelde porties af die na oplossen in water door de patient in gedeelten gespreid over de dag moeten worden ingenomen. Hij stelt de porties als volgt samen
De kritische waarden voor 95% betrouwbaarheid, tweezijdig, bedragen 2,23 bij 10 en 2,26 bij 9 vrijheidsgraden.
gepoolde standaarddeviaties
monster genomen midden boven
monster genomen midden onder
monster genomen zijkant boven
monster genomen zijkant onder
monster genomen midden boven
nvt
1,47
1,47
1,35
monster genomen midden onder
nvt
1,37
1,23
monster genomen zijkant boven
nvt
1,22
monster genomen zijkant onder
nvt
berekende t-waarden
monster genomen midden boven
monster genomen midden onder
monster genomen zijkant boven
monster genomen zijkant onder
monster genomen midden boven
nvt
1,31
2,58
1,60
monster genomen midden onder
nvt
4,16
3,25
monster genomen zijkant boven
nvt
1,19
monster genomen zijkant onder
nvt
Uit de berekende waarden blijkt dat het gehalte aan de zijkant boven significant afwijkt van het gehalte midden boven en midden onder. Het monster dat midden onder genomen is wijkt significant af van het monster dat aan de zijkant onder genomen is. Hieruit blijkt dat er dus geen is sprake van homogene menging.
Voor de bepaling van kalium komt vlamemissiespectrometrie het meest voor de hand.b. chloride
Voor de bepaling van chloride komt een titratie met zilvernitraat in aanmerking.c. gluconaat
Ag + + Cl- = AgCl De reactie kan potentiometrisch gevolgd worden met behulp van een zilverelectrode als indicatorelectrode en een zilver/zilverchloriderefentie-electrode (met dubbele zoutbrug !).
Het eindpunt kan ook vastgesteld worden met kaliumchromaat als indicator (Titratie volgens Mohr).
Een derde mogelijkheid bestaat uit het toevoegen van een overmaat zilver gevolgd door een terugtitratie met kaliumthiocyanaat. Hierbij wordt ferriammoniumsulfaat als indicator gebruikt. Om omzetting van het neergeslagen zilverchloride in zilverthiocyanaat tegen te gaan dient het zilverchloride omhuld te worden met dibutylftalaat (Titratie volgens Volhard).
Het gluconaat kan bepaald worden door een titratie met perchloorzuur in watervrij azijnzuur. Hierbij wordt het gluconaat omgezet in gluconzuur:Vraag 3.R-COO- + H+ = R-COOH Chloride stoort hierbij niet omdat het een veel zwakkere base is dan het gluconaatanion.
Alvorens een monster uit een suspensie te nemen dient de suspensie zo goed mogelijk gemengd te worden, opdat door de monstername de samenstelling van de achterblijvende suspensie niet verandert en een representatief monster verkregen wordt.b. Geef aan op welke wijze u het naproxeen voor een identificatie door middel van infraroodspectrometrie zou isoleren en geef expliciet aan welke voorzorgen u hierbij dient te nemen om een betrouwbaar spectrum te verkrijgen?
Het onopgeloste deel kan door centrifugeren worden verzameld. Na uitwassen met water en drogen kan van het residu een IR-spectrum worden opgenomen.c. Geef aan op welke wijze u naproxeen in dit preparaat UV-spectrometrisch zou bepalen. Geef aan hoeveel van de suspensie u voor deze bepaling in bewerking zou nemen, hoe u de bewerking zou uitvoeren en welke extinctie u verwacht te meten.
Het is ook mogelijk de suspensie met een daarvoor geschikt extractiemiddel als ether of chloroform na aanzuren te extraheren, het extract achtereenvolgens te wassen, over uitgedroogd natriumsulfaat te drogen en in te dampen. Het verkregen residu bevat dan echter nog ongeveer 4% methylparahydroxybenzoaat. Vermoedelijk is deze verontreiniging geen beletsel om een bruikbaar IR-spectrum op te nemen.
Om eventuele basische en neutrale verontreinigingen uit de begeleidende stoffen te verwijderen is het aan te bevelen om de extractie uit zuur milieu vooraf te laten gaan door een extractie uit alkalisch milieu.
Bij een extinctiemeting moet men rekening houden met storingen door het methylparahydroxybenzoaat en de bestanddelen van de klaproosstroop. De storingen door de klaproosstroop kunnen hoogstwaarschijnlijk worden geëlimeneerd door een extractie uit zuur milieu eventueel voorafgegaan door een extractie uit alkalisch milieu zoals beschreven bij de isolatie voor het IR-spectrum.d. Geef aan op welke wijze u naproxeen in dit preparaat via een zuur-base titratie zou kunnen bepalen. Geef aan hoeveel van de suspensie u voor deze bepaling in bewerking zou nemen, hoe u de bewerking zou uitvoeren en hoeveel ml titrans u verwacht te gebruiken.
De aanwezigheid van methylparahydroxybenzoaat geeft in het golflengtegebied van 260 tot 272 nm een storing omstreeks 16% (4% verontreiniging met een ongeveer 4x zo hoge extinctie). Door de meting uit te voeren bij 330 nm kan deze storing vermeden worden (mits niet in alkalisch milieu gemeten wordt !!).
De specifieke extinctie bedraagt bij deze golflengte ongeveer 80.Weeg ongeveer 2 g suspensie af en los deze op in 0,1 M natronloog tot 100,0 ml.
Extraheer 10,0 ml van de verkregen verdunning met chloroform of ether en verwerp de organische laag.
Zuur de waterlaag aan met verdund zwavelzuur en extraheer meermaals met chloroform. Verzamel de chloroformlagen en vul deze aan tot 100,0 ml. Meet de extinctie bij een weglengte van 1 cm. De te verwachten extinctie bedraagt 0,4. Bereken het gehalte door vergelijking met de extinctie van een naproxenoplossing van bekende sterkte (standaardoplossing).
Controleer de aanwezigheid van eventuele storende verontreinigingen door de spectra van de monsteroplossing te vergelijken met die van de standaardoplossing.
Extraheer de overgebleven waterlaag nogmaals en controleer de volledigheid van de extractie.
Een directe titratie met loog is niet aan te bevelen omdat het niet zeker is dat de naproxen tijdens de titratie voldoende snel in oplossing gaat. Beter is het daarom om een overmaat natronloog toe te voegen en de overmaat terug te titreren met zoutzuur. De bepaling zou dan als volgt uitgevoerd kunnen worden: Weeg ongeveer 13 g van de suspensie af, voeg 20,00 ml 0,1 M natronloog toe. Titreer vervolgens met 0,1 N. zoutzuur. stel het eindpunt potentiometrisch vast met behulp van een gecombineerde glaselectrode. Het te titreren volume bedraagt ongeveer 6 ml.e. U beschikt niet over gegevens over het chromatografisch gedrag van naproxeen op met octadecylgroepen gecoat silicagel. U zoekt daarom zelf een bruikbaar loopmiddel. Uw eerste analyse verricht u met een loopmiddel met 80% methanol waaraan 10 mM perchloorzuur is toegevoegd. U meet hierbij een capaciteitsfactor van 0,3. Welke capaciteitsfactor verwacht u bij gebruik van een loopmiddel met 60% methanol met 10 mM perchloorzuur ?
Bij verlaging van het methanogehalte met 10% neemt de capaciteitsfactor in het algemeen met een factor 2 tot 3 toe. Bij 70% methanol bedraagt de capaciteitsfactor dan 0,6 tot 0,9, bij 60% methanol dus 1,2 tot 2,7.f. Geef aan hoe de retentie van naproxeen en van methyloxybenzoaat in dit systeem met de pH van het loopmiddel zouden varieren, wanneer u in plaats van een perchloorzuur bevattend loopmiddel een gebufferd loopmiddel zou gebruiken. Geef bij uw beantwoording grafisch het verband tussen de capaciteitsfactor en de pH weer.
Zuren vertonen retentie in hun geprotoneerde vorm. De ligging van het protolytisch evenwicht wordt bepaald door de pH en de pKa. Het verband tussen de capaciteitsfactor en de pH wordt dientengevolge gegeven door een sigmoidale curve, waarvan het buigpunt bij de pKa ligt. De onderstaande afbeelding illustreert dit.
Hierbij is aangenomen, dat de capaciteitsfactor van het geprotoneerde naproxeen hoger is dan die van methylparahydroxybenzoaat. Eventuele retentie van de anionen in de vorm van ionparen is buiten beschouwing gelaten.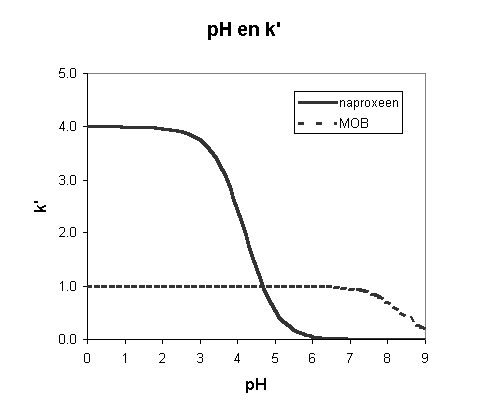
Aan deze uitwerkingen kunnen geen rechten worden ontleend
Farmaceutische Analyse 5e-jaar |
17 januari 2001
Staf Farmaceutische Analyse 5e-jaar